3줄 요약
- 핵심 1: 췌장암(PDAC) 환자 대상 3상에서 다라크소나십 단독 경구 투여가 표준 화학요법 대비 사망위험을 60% 낮췄습니다(NEJM 2026, RASolute 302).
- 핵심 2: 비결은 ‘RAS의 활성형(ON state)’에 직접 결합하는 새로운 작용 기전입니다. 기존 KRAS G12C 약은 췌장암 변이 분포(G12C 1~2%)와 어긋나 사실상 도움이 안 됐습니다.
- 핵심 3: 한국 췌장암 5년 생존율은 15.9%로 모든 암 중 최저입니다. 그래서 이 약의 의미가 더 무겁습니다.
1. 췌장암 평균 생존이 처음으로 두 배가 됐다
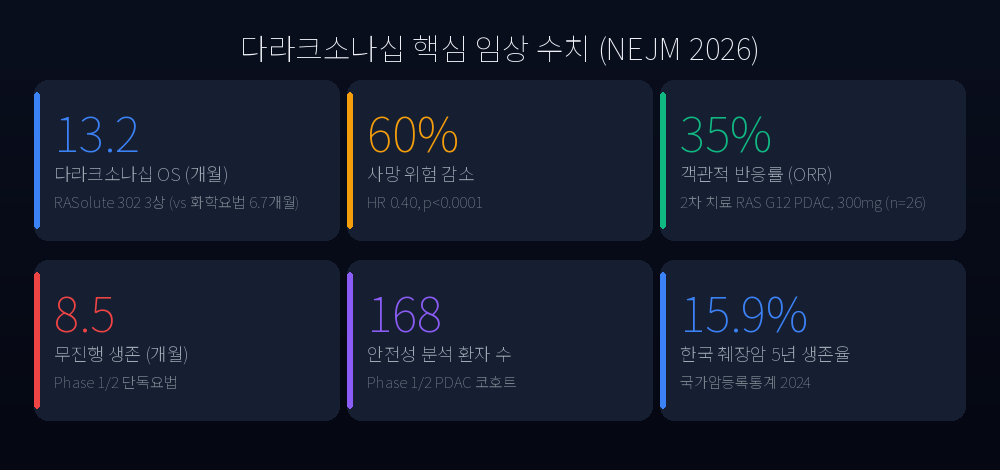
2026년 5월 7일, New England Journal of Medicine에 다라크소나십(daraxonrasib, RMC-6236)의 췌장암 임상 결과가 실렸습니다(Wolpin et al., NEJMoa2505783). 이어 같은 달 발표된 글로벌 3상 RASolute 302는 더 인상적인 숫자를 보여줬습니다. 다라크소나십을 받은 환자의 중앙 전체생존(OS)은 13.2개월, 표준 화학요법군은 6.7개월. 사망위험비(HR)는 0.40(p<0.0001), 즉 사망위험이 60% 낮아졌습니다.
췌장암 분야에서 ‘두 배’라는 단어가 등장하는 일은 거의 없습니다. 1996년 젬시타빈(gemcitabine) 도입 이후 30년 동안 2차 치료 OS는 6~8개월 수준에서 멈춰 있었고, 2011년 FOLFIRINOX, 2013년 nab-paclitaxel 병용요법조차도 이 한계선을 깨지 못했습니다. 그래서 이번 결과는 단순한 ‘신약 출시’가 아니라 ‘표적이 잘못 잡혀 있었다’는 패러다임 전환의 신호입니다.
2. 왜 RAS는 30년간 ‘약물화 불가능’한 표적이었나
RAS 단백질은 세포 성장 신호의 중앙 스위치입니다. 정상 상태에서는 GDP가 결합한 OFF 상태와 GTP가 결합한 ON 상태를 오가지만, 변이가 생기면 ON 상태에 고착돼 끊임없이 증식 신호를 보냅니다. 췌장관선암(PDAC)의 경우 90% 이상에서 KRAS 변이가 확인됩니다.
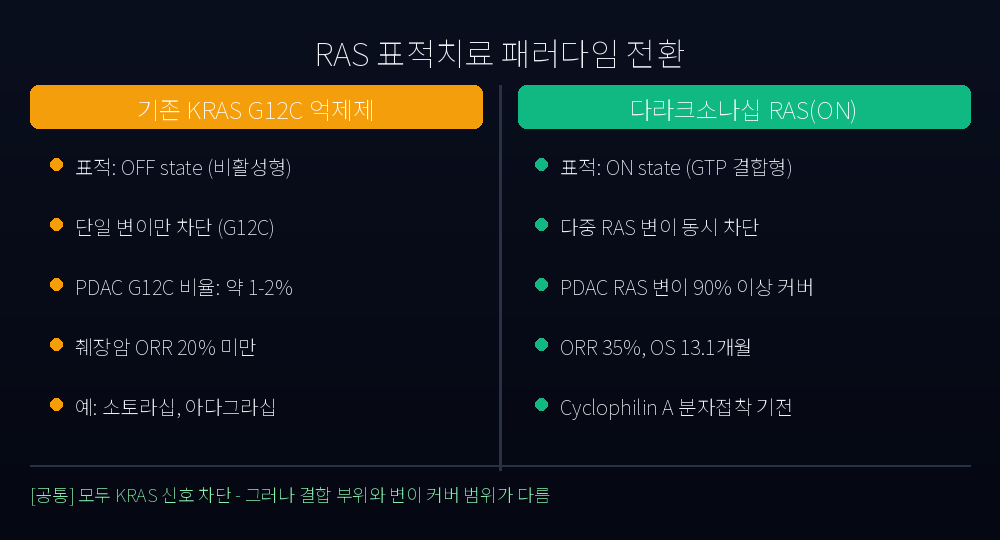
문제는 RAS의 표면이 너무 평탄하다는 점이었습니다. 분자생물학자들이 1980년대부터 약물의 결합 포켓을 찾았지만 적당한 ‘주머니’가 없었습니다. 2021년 FDA는 첫 KRAS 표적약 소토라십(sotorasib)을 폐암용으로 승인했지만, 이는 G12C 변이의 시스테인(C) 잔기에 공유결합하는 매우 좁은 표적이었습니다.
여기에 결정적 함정이 있었습니다. PDAC의 RAS 변이 분포는 G12D 약 41%, G12V 약 30%, G12R 약 17%로 압도적이고, G12C는 1~2%에 불과합니다(Bryant et al., 2014; Waters & Der, 2018). 결국 폐암에서 효과가 입증된 약이 췌장암 환자 대다수에게는 처음부터 맞지 않는 열쇠였던 셈입니다.
다라크소나십이 다른 점은 두 가지입니다. 첫째, OFF가 아닌 ON 상태(GTP 결합형)에 결합합니다. 둘째, 단일 변이가 아니라 G12 계열 다수 + 야생형 RAS까지 동시에 표적합니다. 작용 기전은 ‘분자 접착제(molecular glue)’ 형태로, 약물이 세포 내 단백질 사이클로필린 A(cyclophilin A)와 먼저 복합체를 만든 뒤 활성형 RAS 표면에 달라붙어 하류 신호 전달(MAPK/ERK)을 차단합니다.

3. 임상 데이터 깊이 보기 - 좋은 숫자, 그러나 조건이 있다
연구 설계와 핵심 결과
NEJM에 실린 phase 1/2 연구는 이전에 화학요법을 받은 RAS 변이 PDAC 환자 168명을 대상으로 10mg에서 400mg까지 용량을 단계별로 평가했습니다. 권장 3상 용량으로 선정된 300mg 1일 1회 경구 투여, 2차 치료 단독요법 코호트(n=26, RAS G12 변이)에서:
- 객관적 반응률(ORR): 35% (95% CI 17~56%)
- 중앙 무진행생존(PFS): 8.5개월 (95% CI 6.7~10.5)
- 중앙 전체생존(OS): 13.1개월 (95% CI 10.9~NE)
이어 발표된 phase 3 RASolute 302는 동일 인구를 표준 화학요법(FOLFIRI 또는 mFOLFOX 등 의사 선택)과 1:1 무작위 배정한 글로벌 시험으로, 1차 평가변수인 OS와 PFS 모두 통계적으로 유의한 개선을 입증했습니다. ITT 인구 OS 13.2 vs 6.7개월, HR 0.40, p<0.0001. 1차 치료 코호트의 추적 13.7개월 시점 ORR은 47%, 6개월 PFS 71%로 보고됐습니다.
안전성 - 솔직한 평가
낙관만 전하면 위험합니다. 168명 PDAC 코호트에서 치료 관련 부작용은 전등급 96%, 등급 3 이상이 30%였습니다. 가장 흔한 부작용은 다음과 같습니다.
- 발진(rash): 91%
- 설사: 48%
- 오심: 43%
- 구토: 31%
- 구내염/점막염: 31%
- 피로: 20%
- 조갑주위염(paronychia): 13%
발진이 91%라는 수치는 기존 EGFR 표적치료(약 70~80%)보다 높은 수준입니다. 이는 다라크소나십이 정상 세포의 야생형 RAS도 일부 차단하기 때문으로 추정되며, 일부 환자에게는 용량 조절이나 일시 중단이 필요할 수 있습니다. 주치의의 면밀한 모니터링이 전제된 약물입니다.
한계 - 아직 묻지 못한 질문
- 1차 치료 데이터는 phase 1/2 단독·병용 코호트에서 ORR 47%로 인상적이지만 추적기간이 짧고 무작위 비교가 없습니다.
- 2차 단독요법 ORR 35% 코호트의 표본이 26명으로 작아 신뢰구간이 17~56%로 넓습니다.
- 장기 내성 기전은 거의 알려진 바가 없습니다. 다른 표적치료처럼 ctDNA 기반 RAS 변이 변천이 나올 가능성이 큽니다.
- 비RAS G12 변이(Q61, A146 등) 효과는 추가 분석이 필요합니다.
4. 한국인에게 주는 시사점 - 왜 이 뉴스를 더 무겁게 봐야 하나
한국 보건복지부·중앙암등록본부의 2024년 발표(2022년 기준 통계)에 따르면 한국의 췌장암 5년 상대생존율은 약 15.9%로 주요 암 중 최저입니다. 같은 자료에서 위암 78.0%, 갑상선암 100.1%(인구집단 기준 사망률 보정), 대장암 74.3%와 비교하면 격차가 명확합니다. 매년 약 9,800명이 새로 진단받고, 발견 시 이미 절반 이상이 절제 불가능한 진행 단계입니다.
기존 한국 표준 2차 치료는 1차에 무엇을 썼느냐에 따라 다음 중 선택됩니다.
- 1차 FOLFIRINOX → 2차 nab-paclitaxel + gemcitabine (또는 5-FU 기반)
- 1차 gemcitabine + nab-paclitaxel → 2차 oxaliplatin/irinotecan 기반(NAPOLI/MM-398 포함)
이들 2차 요법의 보고된 OS는 6~8개월 선이며, FOLFIRI 단독의 한국 다기관 데이터에서도 비슷한 범위입니다(대한종양내과학회 권고안 2023). 다라크소나십의 13.2개월 OS는 이 한국 표준의 약 2배입니다.
다만 한국 임상 도입에는 현실적 시차가 있습니다.
- FDA 승인은 2026년 후반~2027년 초로 예상되며, 식약처 도입은 통상 6~18개월 추가 소요.
- RAS 변이 검사가 보험 급여 항목으로 자리 잡아야 합니다. 현재 한국 췌장암 치료 시 KRAS 시퀀싱은 임상시험 외에는 표준이 아닙니다.
- 약가 협상 - GLP-1 약(위고비, 마운자로) 사례처럼 2~3년 협상 지연 가능성이 있습니다.
- 가족력 췌장암(BRCA, PALB2 변이 보유자)의 한국인 비율은 전체의 5~10%로 추정되며, 이들 인구의 1차 PARP 억제제(올라파립) 등 기존 표적치료 데이터와 어떻게 결합될지가 추가 과제입니다.
5. 환자와 가족이 지금 할 수 있는 것
긍정적인 임상 데이터가 나왔다고 해서 당장 표준 치료를 흔들 필요는 없습니다. 다만 몇 가지를 점검해두는 건 의미가 있습니다.
-
정확한 변이 검사 요청. 진단 시 또는 1차 치료 실패 후 KRAS 변이형(G12D/V/R/C 등) 분석을 주치의에게 요청하세요. 이는 다라크소나십뿐 아니라 향후 RAS 표적치료 전반의 적용 가능성을 좌우합니다. 검사는 종양 조직 또는 혈액 ctDNA로 가능합니다.
-
임상시험 등록 검토. RASolute 302 이후 한국에서도 다라크소나십 또는 후속 RAS(ON) 약물(예: 동일 회사의 RMC-6291 G12C ON-state 약)의 임상이 시작될 가능성이 큽니다. 국립암센터·서울대병원·삼성서울병원 종양내과에 등록 가능한 시험을 문의하거나 ClinicalTrials.gov에서 ‘daraxonrasib Korea’ 또는 ‘RMC-6236’을 검색하세요.
-
표준치료 임의 중단 금지. 신약 데이터를 보고 현재 효과를 보이는 화학요법을 중단하는 것은 위험합니다. 임상시험 입장 시점은 보통 표준치료 진행 또는 부작용으로 중단 시점입니다.
-
부작용 사전 학습. 다라크소나십의 발진 91%, 설사 48%는 결코 가벼운 수치가 아닙니다. 실제 처방이 시작되면 피부과·소화기내과 협진이 동반되어야 할 가능성이 높습니다. 보호자도 부작용 관리 매뉴얼을 미리 확인할 가치가 있습니다.
-
가족력 점검과 조기 발견. 췌장암은 1차 친족 중 환자 2명 이상 시 위험이 약 6.4배(National Familial Pancreatic Tumor Registry, 2018)로 보고됐습니다. 50세 이상 또는 가족력 보유자는 복부 MRI/MRCP를 통한 정기 검진을 주치의와 상의하세요. 췌장암 조기 발견은 여전히 다라크소나십을 포함한 모든 약물 효과를 결정짓는 가장 강력한 변수입니다.
6. 정리 - 신중한 낙관
다라크소나십의 의의를 한 줄로 요약하면 이렇습니다. ‘30년 동안 헛 표적을 겨눠 왔다’는 사실의 첫 임상적 증거. RAS는 약물화 불가능한 표적이 아니었고, 단지 우리가 잘못된 상태(OFF state)와 잘못된 변이(G12C 단일)를 노리고 있었을 뿐입니다.
물론 신중함은 필수입니다. 이번 데이터는 2차 치료 환자 26명, 3상 ITT 인구가 추적 중이며, 1차 치료 데이터와 장기 내성, 한국인 변이 분포 적합도는 추가 검증이 필요합니다. 그래도 췌장암이라는, 의료계가 가장 두려워해온 암의 벽에 처음으로 균열이 생긴 것은 분명합니다.
다음 1~2년이 결정적입니다. RASolute 302의 최종 분석(2026 ASCO 발표 예정), FDA 신속 승인, 그리고 한국 식약처 신청과 보험 급여 협상이 어떻게 풀리느냐에 따라 한국 환자가 실제로 이 약을 쓸 수 있는 시점이 정해집니다.
본 콘텐츠는 건강 정보 제공 목적이며, 의학적 진단이나 치료를 대체하지 않습니다. 췌장암을 포함한 모든 암 치료 결정은 반드시 담당 종양내과 전문의와 상담 후 내려주세요. 임상시험 참여 결정도 마찬가지입니다.
