3줄 요약
- 핵심 1: 단 1회 정맥 주입으로 LDL 콜레스테롤을 평균 53%(최대 69%) 영구적으로 낮춘 임상 결과가 Nature Medicine 2026년 5월호에 발표됐습니다.
- 핵심 2: ‘CRISPR 절단’ 방식이 아니라 DNA 한 글자(A→G)만 바꾸는 염기 교정(base editing) 방식으로, 14명 시험 참가자 전원에서 치료 관련 중대 이상반응이 보고되지 않았습니다.
- 핵심 3: 한국 가족성 고지혈증(FH) 환자 약 25만 명 중 스타틴 최대 용량으로도 LDL 목표에 도달하는 비율은 11.5%에 불과합니다. ‘평생 매일 약’이라는 패러다임이 흔들리고 있습니다.
1. 단 한 번의 주사로 평생 LDL을 53% 낮춘다는 임상 결과
Verve Therapeutics가 진행한 Heart-2 Phase 1b 임상시험의 1차 결과가 2026년 Nature Medicine에 보고됐습니다(Verve Therapeutics, 2025; Khoja et al., Nature Medicine, 2026).
연구진은 가족성 고지혈증(Heterozygous Familial Hypercholesterolemia, HeFH) 또는 조기 관상동맥질환을 가진 성인 14명에게 VERVE-102라는 단일 정맥 주사를 투여했습니다. 결과는 다음과 같습니다.
- 0.3 mg/kg 용량: 평균 LDL-C 21% 감소, PCSK9 단백 46% 감소
- 0.45 mg/kg 용량: 평균 LDL-C 41% 감소, PCSK9 단백 53% 감소
- 0.6 mg/kg 용량: 평균 LDL-C 53% 감소, 최대 69% 감소, PCSK9 단백 60% 감소
치료 관련 중대 이상반응(SAE)은 0건, 임상적으로 의미 있는 검사 이상도 0건이었습니다. Grade 2 주입 관련 반응이 1건 있었으나 아세트아미노펜으로 호전됐습니다(Verve Therapeutics IR, 2025).
기존 스타틴은 매일 복용해야 효과가 유지됩니다. PCSK9 단클론항체(Repatha, Praluent)는 2주에 한 번 피하 주사가 필요합니다. siRNA 치료제(Inclisiran)는 6개월마다 주사가 필요합니다. VERVE-102는 단 한 번의 주입으로 효과가 지속되도록 설계됐다는 점에서 패러다임이 다릅니다.

2. 한국 FH 환자 25만 명의 현실 — 왜 ‘평생 1회’가 중요한가
가족성 고지혈증(FH)은 LDL 수용체 또는 PCSK9 유전자 변이로 인해 혈중 LDL이 평생 높게 유지되는 유전 질환입니다. 전 세계 유병률은 약 1/200~1/500로 추정되며, 한국에는 약 10만~25만 명의 환자가 있는 것으로 추산됩니다(Korean Society of Lipid and Atherosclerosis, 2022).
한국 다기관 실제 임상 데이터(Multicenter Real-world Experience)에 따르면:
- FH 환자의 등록 시 평균 LDL-C는 247 ± 98 mg/dL (한국지질·동맥경화학회 코호트).
- 최대 강도 스타틴 + 에제티미브 병용 1년 후 평균 LDL-C는 122 ± 60 mg/dL.
- 가이드라인 권장 목표(LDL-C < 100 mg/dL)에 도달한 비율은 11.5%.
- PCSK9 단클론항체를 사용 중인 환자 비율은 11.7% (가격·접근성 문제).
즉 한국 FH 환자의 약 88%는 가장 강력한 경구 치료를 최대 용량으로 받고도 목표 LDL에 도달하지 못합니다. PCSK9 항체는 효과는 좋지만 2주마다 주사를 맞아야 하고 비급여 본인부담이 크기 때문에 사용률이 낮습니다.
‘단 1회 주사로 평생 LDL을 절반 가까이 낮춘다’는 가설이 검증된다면, 이는 단순한 약물 추가가 아니라 치료 접근성 자체를 다시 정의하는 시도입니다.
3. 메커니즘: A를 G로 단 한 글자만 바꾸는 ‘염기 교정’이란 무엇인가
이 부분이 일반 CRISPR 치료와의 결정적 차이입니다. 깊이 있게 봅시다.
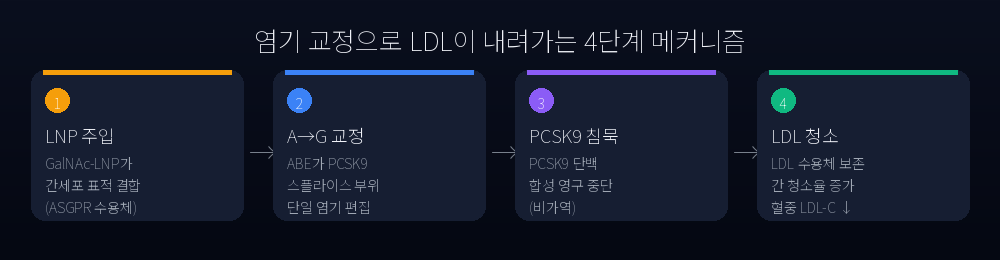
전체 경로 (A→B→C→D→E→F)
- 간 표적 전달: VERVE-102는 GalNAc(N-아세틸갈락토사민) 분자가 표면에 부착된 지질 나노입자(LNP) 형태입니다. GalNAc는 간세포 표면에 풍부한 ASGPR(asialoglycoprotein receptor) 수용체와 특이적으로 결합해, 약물이 간세포에만 집중 흡수되도록 합니다(Springer et al., NEJM 2018; Verve mechanism review, Tandfonline 2024).
- 세포 내 방출: 간세포 내부로 들어간 LNP는 분해되며, 안에 담긴 mRNA(아데닌 염기 편집기, ABE를 코딩)와 가이드 RNA(sgRNA)가 방출됩니다.
- 표적 탐색: ABE-sgRNA 복합체는 PCSK9 유전자의 엑손 1에 있는 표준 스플라이스 부위(canonical splice site)를 정확히 찾아냅니다.
- 한 글자 편집: ABE는 DNA를 자르지 않습니다. 대신 표적 위치의 아데닌(A) 염기에서 아미노기를 떼어내 이노신(I)으로 변환합니다. 이노신은 DNA 복제 시 구아닌(G)처럼 읽히므로, 결과적으로 ‘A→G’ 한 글자 교정이 일어납니다(Anzalone et al., Nature 2019; Verve VERVE-101 paper, 2024).
- PCSK9 단백 침묵: 스플라이스 부위가 망가지면 PCSK9 mRNA가 정상적으로 만들어지지 못합니다. 그 결과 PCSK9 단백 합성이 영구적으로 차단됩니다.
- LDL 청소 가속: PCSK9의 본래 역할은 간세포 표면의 LDL 수용체(LDLR)를 분해 경로로 보내는 것입니다. PCSK9가 사라지면 LDLR이 분해되지 않고 표면에 더 오래 머무릅니다. 표면에 LDLR이 많아지면 혈중 LDL 입자를 더 빠르게 청소합니다. → 혈중 LDL-C 감소.
CRISPR-Cas9 절단형 편집은 DNA를 양쪽으로 자르고 세포가 이를 어떻게든 다시 붙이는데, 이 과정에서 큰 결실(deletion)이나 전위(translocation) 같은 부작용 우려가 있습니다. 염기 교정은 절단하지 않고 한 글자만 바꾸기 때문에 이론적으로 안전성 프로파일이 다릅니다. Heart-2에서 14명 전원에 SAE가 없었다는 데이터는 이 가설을 일차적으로 뒷받침합니다.
4. 한국인 관점 — 매일 약과 단회 주사 사이
한국인의 식습관과 의료 시스템 관점에서 이 연구가 시사하는 바를 봅시다.
- 순응도 문제: 한국 만성질환 통계에 따르면 고지혈증 약을 1년 후에도 꾸준히 복용하는 환자 비율은 50~60% 수준입니다(건강보험심사평가원 만성질환 적정성 평가). 매일 약 먹기가 어렵다는 현실은 한국도 다르지 않습니다.
- 비급여 부담: 한국에서 PCSK9 단클론항체(예보로큐맙·알리로쿠맙)는 일부 조건(FH 확진, 죽상경화증 동반)에 한해 산정특례나 보험 적용이 가능하지만, 일반 고지혈증에는 비급여로 연간 수백만 원 본인부담이 발생합니다.
- 심혈관 질환 부담: 통계청 사망원인 통계에서 심장질환은 한국 사망원인 2위(2024년 기준, 인구 10만 명당 약 65명)입니다. LDL은 가장 큰 수정 가능한 위험인자입니다.
VERVE-102가 향후 글로벌 Phase 3에서 효과·안전성을 재확인하고 허가에 이른다면, 한국에서도 다음 질문이 곧 의제가 됩니다: ‘평생 1회 주사’ 약물의 가격을 사회가 어떻게 받아들일 것인가? 매일 복용하는 스타틴은 연간 수만 원이지만, 단회 유전자 편집 치료는 미국에서 50~100만 달러 수준으로 책정될 가능성이 있습니다(Cell & Gene Therapy 시장 분석, 2025). 단순 가격만 비교하면 비싸 보이지만, 평생 LDL 관리에 들어가는 누적 의료비, 심혈관 사건 예방 효과까지 고려하면 비용-효과 분석이 필요한 영역입니다.

5. 한계와 주의사항 — 흥분 전에 알아야 할 5가지
이 연구는 매우 중요한 1보(first-in-human)이지만, 다음 사실을 함께 알아야 합니다.
- 표본이 작습니다: Phase 1b는 안전성 확인을 위한 초기 시험으로, 14명의 데이터만으로 일반 환자에게 권할 수 있는 단계가 아닙니다.
- 추적 기간이 짧습니다: 1차 결과는 단기 추적입니다. ‘평생 지속’은 동물 모델에서 시사되지만, 사람에서 10년·20년 효과는 후속 연구로 확인해야 합니다.
- 비가역적입니다: 한 번 편집된 PCSK9 유전자는 되돌릴 수 없습니다. 만약 장기적으로 예상치 못한 부작용(예: PCSK9 완전 결손과 관련된 인지 기능 변화 가능성에 대한 학계 논쟁)이 발견된다면, 약을 끊는 식의 대응이 불가능합니다(NEJM Loss-of-function PCSK9 cohort, 2006 vs Schmidt et al., Lancet Diabetes Endocrinol 2017 논쟁 참고).
- 임상 단계입니다: 현재 일반 진료에서 처방되지 않습니다. 미국 FDA 허가는 빨라도 2028~2030년경으로 예상됩니다.
- 모두에게 필요한 것이 아닙니다: FH나 약물 불응성 고LDL 환자에게 우선 검토되는 치료입니다. 스타틴으로 잘 조절되는 일반 고지혈증 환자에게는 굳이 권장될 이유가 약합니다.
6. 지금 우리가 할 수 있는 것 — 구체적 행동 가이드
이 신약을 기다리는 것보다 더 중요한 것은 자신의 LDL 수치와 가족력을 정확히 아는 것입니다.
- 가족력 점검 (10분, 무료): 부모·형제자매 중 55세 이전(남성), 60세 이전(여성) 심근경색·뇌졸중 병력이 있다면 FH 가능성을 의심합니다. 본인의 LDL이 미치료 시 190 mg/dL 이상이면 더욱 의심도가 높아집니다(Dutch Lipid Clinic Network 기준). 의사에게 ‘FH 의심된다’고 말하면 유전자 검사 의뢰가 가능합니다.
- 현재 LDL 목표 확인 (5분): 한국지질·동맥경화학회 2022 가이드라인에 따르면 초고위험군(관상동맥질환 동반)은 LDL-C < 55 mg/dL, 고위험군은 < 70 mg/dL, 중간 위험군은 < 100 mg/dL이 목표입니다. 본인의 검사 결과지에서 LDL이 이 목표에 도달했는지 확인하세요.
- 스타틴 순응도 점검: 최근 1개월간 처방받은 약을 며칠 빠뜨렸는지 솔직히 셉니다. 30일 중 5일 이상 빠뜨렸다면 약사·의사에게 알리고 복용 시간 조정 등을 상의하세요. 순응도 80% 미만은 약 효과의 약 30%를 잃는 것과 같다는 연구가 있습니다(Lansberg et al., Vascular Health Risk Manag 2018).
- 식이 — ‘나트륨 제한’보다 ‘포화지방·트랜스지방 제한’이 LDL에는 더 직접적: 한국인의 평균 포화지방 섭취는 일일 권장량(총 열량의 7% 이하)을 약 1.5배 초과합니다(국민건강영양조사). 라면 국물, 가공육, 빵·과자류 섭취 빈도를 줄이면 4~6주 내 LDL이 평균 10~15% 감소한다는 결과가 있습니다(Hooper et al., Cochrane Review 2020).
- 운동 — 유산소 + 저항운동 병행: 주 150분 중강도 유산소 운동 + 주 2회 저항운동이 LDL을 6~10% 낮추는 것으로 보고됩니다(Kelley et al., J Lipid Res 2014). 단기간에 LDL을 큰 폭으로 낮추지는 못하지만 HDL 상승과 인슐린 감수성 개선 효과가 있습니다.
VERVE-102의 임상은 계속 진행 중이며, ClinicalTrials.gov(NCT05996940)에서 진행 상황을 확인할 수 있습니다. 한국 환자가 글로벌 Phase 3에 참여할 수 있는 기관이 향후 발표될 가능성이 있어 모니터링 가치가 있습니다.
한 줄 결론
평생 매일 약을 먹어야 했던 콜레스테롤 치료가, ‘단 한 번의 편집’으로 대체될 수 있다는 첫 임상 신호가 나왔습니다. 다만 14명, 단기 데이터입니다. 흥분도 공포도 아닌 차분한 추적이 필요한 시점입니다.
관련 제품
- 오메가3 — 심혈관 건강과 관련된 오메가3 지방산 보충제
이 포스팅은 쿠팡 파트너스 활동의 일환으로, 이에 따른 일정액의 수수료를 제공받습니다.
본 콘텐츠는 건강 정보 제공 목적이며, 의학적 진단이나 치료를 대체하지 않습니다. 건강에 관한 결정은 반드시 전문 의료인과 상담 후 내려주세요.
참고 자료
- Verve Therapeutics. Positive Initial Data from the Heart-2 Phase 1b Clinical Trial of VERVE-102. April 14, 2025.
- Nature Medicine Editorial. Base editing milestone for familial hypercholesterolemia. Nature Medicine, 2026.
- Korean Society of Lipid and Atherosclerosis. 2022 Consensus Statement on the Management of Familial Hypercholesterolemia in Korea. Korean J Intern Med, 2022.
- Kim et al. Target achievement with maximal statin-based lipid-lowering therapy in Korean patients with familial hypercholesterolemia. J Clin Lipidol, 2019.
- Anzalone et al. Search-and-replace genome editing without double-strand breaks or donor DNA. Nature, 2019.
- Hooper et al. Reduction in saturated fat intake for cardiovascular disease. Cochrane Database Syst Rev, 2020.
